がん細胞だけを選択的に破壊 ホウ素中性子捕捉療法 次世代粒子線治療の現状と展望 学会長の平塚純一・川崎医大教授に聞く
川崎医大病院(倉敷市松島)が2003年から放射線治療の臨床研究で、難治性の頭頸部(とうけいぶ)がんと皮膚がん(悪性黒色腫)に「ホウ素中性子捕捉療法」(BNCT)を行っている。岡山県外の中性子照射施設を利用、がん細胞だけを選択的に破壊する。体の負担が少ない独創的な治療法といわれる。日本中性子捕捉療法学会長を務める平塚純一・同大放射線医学(治療)教授=写真=に原理や治療方法、BNCTの動向について聞いた。
------------------------
原理
核分裂反応で粒子線発生 正常細胞ほぼダメージなし
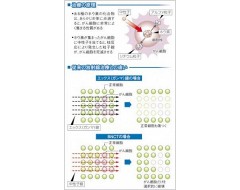
ある種のホウ素化合物は、あらかじめ体に点滴すると、がん細胞に非常によく集まる性質がある。ホウ素は中性子が当たると核分裂を起こし、細胞を死滅させる能力を持つアルファ粒子(ヘリウム原子)が発生する。そのアルファ粒子の飛ぶ距離はわずか10マイクロメートル(1マイクロメートルは千分の1ミリ)。
「核分裂反応というとどうしても核爆弾のイメージがあり、その影響(エネルギー)は何キロにも及ぶと思ってしまうが、BNCTでのアルファ粒子のエネルギーはがん細胞1個の直径に等しい距離しか及ばないのです」と平塚教授は解説する。
がん細胞にのみホウ素が取り込まれ、周囲の正常細胞にホウ素が取り込まれなければ、中性子照射によりホウ素が存在するがん細胞の所でのみ核分裂反応が生じ、その影響は隣の正常細胞には届かないことになる。「がん細胞の中だけで全てのイベントは完結する。『がん細胞選択性治療』『次世代粒子線治療』とも言われます」と平塚教授はBNCTの特徴を語る。
がん病巣はCT(コンピューター断層撮影装置)やMRI(磁気共鳴画像装置)によって画像として観察できるが、実際は病巣の周りに画像では見えないがんの広がりがあり、がん細胞と正常細胞は混在している。
従来の高エネルギーエックス線や陽子線・炭素線治療で治療を行う場合は、正常細胞を含む広い範囲に照射しなければならず、がん細胞の間に存在する正常細胞も傷つき、それが副作用につながってきた。
BNCTは正常細胞とがん細胞を区別し、がん細胞だけを選択的に死滅させる。しかも、従来の放射線治療は放射線に対する感受性の有無で治療効果が左右されるのに対し、BNCTはホウ素が集積されれば感受性に関係なくがん細胞を破壊できる。通常の放射線治療が効かないがんにも効果が期待できるという。
患者に投与するホウ素化合物は、必須アミノ酸のチロシンにホウ素原子が結合したもので、がん細胞がアミノ酸を取り込みやすい性質を利用している。悪性黒色腫では、アミノ酸の取り込みやすさに加え、チロシンがメラニン合成の前駆物質(前段階の原料)であることから、より集積しやすい。
------------------------
治療
頭頸部がん、皮膚がんに 原則1回照射で治療終了
がんの標準治療は手術、放射線治療、抗がん剤治療を組み合わせて行う。頭頸部がんと皮膚がんのうち、標準治療で効果が期待できない難治性・再発がんが川崎医大病院のBNCTの対象だ。
治療の流れは、患者に標準治療の説明をした上で、BNCTが研究的な治療である旨を説明。書面で同意が得られた後、病巣部へのホウ素集積濃度を調べなければならない。ホウ素化合物を用いたPET(陽電子放射断層撮影)検査を行い、がんへのホウ素集積を測定する。この検査で「BNCTの効果があるかどうかを事前に評価できる」と平塚教授。病巣部のホウ素濃度が周辺正常組織の2・5倍以上あること(川崎医大での基準)が必須条件となる。適応条件を満たせば、治療実施日を決定する。
患者は照射前日、主治医団と共に京都大学原子炉実験所(大阪府熊取町)か日本原子力研究開発機構(茨城県東海村)に移動する。照射当日は、照射2時間前からホウ素化合物を2時間かけて点滴投与し、患者を最適な照射体位に固定した状態で照射を開始する。照射時間は30〜60分。治療は1回照射が原則。照射終了後、川崎医大病院へ戻り経過観察のため1週間入院する。治療スケジュールの細部は、BNCT実施施設、対象疾患により異なる。
平塚教授は「治療同意日から治療実施日まで約4週間かかる」と言い、治療実績について「03年から昨年までに53例に治療を行い、局所のがんはほぼ全例で消失や縮小効果があった」と話す。
□
BNCTに保険適応はなく、臨床研究にかかる費用は研究費で賄われる。1回の治療に医師や原子炉を運転する人まで50人以上が関わる。研究用原子炉が保守点検などで稼働していない場合、治療はできない。治療についての問い合わせは、川崎医大病院(086―462―1111)放射線科(治療)の平塚教授へ。
------------------------
BNCTの動向
BNCTの動向 日本の研究が世界リード 原子炉に代わる加速器開発
BNCTは、中性子の発見から4年後の1936年に米国で原理が提唱された。その臨床研究は60年代後半から、日本が世界をリードする形で発展させてきた。
医用原子力技術研究振興財団(東京)によると、2009年1月までに行われたBNCTの治療は国内で525例を数える。治療対象は脳腫瘍、頭頸部がん、皮膚がん、肝臓がん、肺がん、中皮腫、骨・軟部肉腫など。このうち皮膚がん(悪性黒色腫)治療の実施医療機関は全国で川崎医大病院だけ。
BNCTに用いる中性子はこれまで研究用原子炉からしか得られなかった。原子炉は元来医療設備ではなく、保守点検のための長期休止期間、設置場所の制約などがあり、医療として認められるのは不可能に近い。このため原子炉に代わる中性子源として、小型加速器の開発が行われている。加速器は原子炉よりも操作が簡単で、都市の病院内にも設置可能だ。
今年6月から京都大学原子炉実験所で加速器を使ったBNCTの臨床研究が始まる予定。国立がん研究センター中央病院(東京)も昨年1月、「病院設置型の加速器を開発し3年後をめどに臨床研究を開始する」と発表した。平塚教授は「加速器が本格稼働するようになれば、BNCTが一般的治療として、がん治療の一翼を担える日も近い」と言う。
※登場する人物・団体は掲載時の情報です。
------------------------
原理
核分裂反応で粒子線発生 正常細胞ほぼダメージなし
ある種のホウ素化合物は、あらかじめ体に点滴すると、がん細胞に非常によく集まる性質がある。ホウ素は中性子が当たると核分裂を起こし、細胞を死滅させる能力を持つアルファ粒子(ヘリウム原子)が発生する。そのアルファ粒子の飛ぶ距離はわずか10マイクロメートル(1マイクロメートルは千分の1ミリ)。
「核分裂反応というとどうしても核爆弾のイメージがあり、その影響(エネルギー)は何キロにも及ぶと思ってしまうが、BNCTでのアルファ粒子のエネルギーはがん細胞1個の直径に等しい距離しか及ばないのです」と平塚教授は解説する。
がん細胞にのみホウ素が取り込まれ、周囲の正常細胞にホウ素が取り込まれなければ、中性子照射によりホウ素が存在するがん細胞の所でのみ核分裂反応が生じ、その影響は隣の正常細胞には届かないことになる。「がん細胞の中だけで全てのイベントは完結する。『がん細胞選択性治療』『次世代粒子線治療』とも言われます」と平塚教授はBNCTの特徴を語る。
がん病巣はCT(コンピューター断層撮影装置)やMRI(磁気共鳴画像装置)によって画像として観察できるが、実際は病巣の周りに画像では見えないがんの広がりがあり、がん細胞と正常細胞は混在している。
従来の高エネルギーエックス線や陽子線・炭素線治療で治療を行う場合は、正常細胞を含む広い範囲に照射しなければならず、がん細胞の間に存在する正常細胞も傷つき、それが副作用につながってきた。
BNCTは正常細胞とがん細胞を区別し、がん細胞だけを選択的に死滅させる。しかも、従来の放射線治療は放射線に対する感受性の有無で治療効果が左右されるのに対し、BNCTはホウ素が集積されれば感受性に関係なくがん細胞を破壊できる。通常の放射線治療が効かないがんにも効果が期待できるという。
患者に投与するホウ素化合物は、必須アミノ酸のチロシンにホウ素原子が結合したもので、がん細胞がアミノ酸を取り込みやすい性質を利用している。悪性黒色腫では、アミノ酸の取り込みやすさに加え、チロシンがメラニン合成の前駆物質(前段階の原料)であることから、より集積しやすい。
------------------------
治療
頭頸部がん、皮膚がんに 原則1回照射で治療終了
がんの標準治療は手術、放射線治療、抗がん剤治療を組み合わせて行う。頭頸部がんと皮膚がんのうち、標準治療で効果が期待できない難治性・再発がんが川崎医大病院のBNCTの対象だ。
治療の流れは、患者に標準治療の説明をした上で、BNCTが研究的な治療である旨を説明。書面で同意が得られた後、病巣部へのホウ素集積濃度を調べなければならない。ホウ素化合物を用いたPET(陽電子放射断層撮影)検査を行い、がんへのホウ素集積を測定する。この検査で「BNCTの効果があるかどうかを事前に評価できる」と平塚教授。病巣部のホウ素濃度が周辺正常組織の2・5倍以上あること(川崎医大での基準)が必須条件となる。適応条件を満たせば、治療実施日を決定する。
患者は照射前日、主治医団と共に京都大学原子炉実験所(大阪府熊取町)か日本原子力研究開発機構(茨城県東海村)に移動する。照射当日は、照射2時間前からホウ素化合物を2時間かけて点滴投与し、患者を最適な照射体位に固定した状態で照射を開始する。照射時間は30〜60分。治療は1回照射が原則。照射終了後、川崎医大病院へ戻り経過観察のため1週間入院する。治療スケジュールの細部は、BNCT実施施設、対象疾患により異なる。
平塚教授は「治療同意日から治療実施日まで約4週間かかる」と言い、治療実績について「03年から昨年までに53例に治療を行い、局所のがんはほぼ全例で消失や縮小効果があった」と話す。
□
BNCTに保険適応はなく、臨床研究にかかる費用は研究費で賄われる。1回の治療に医師や原子炉を運転する人まで50人以上が関わる。研究用原子炉が保守点検などで稼働していない場合、治療はできない。治療についての問い合わせは、川崎医大病院(086―462―1111)放射線科(治療)の平塚教授へ。
------------------------
BNCTの動向
BNCTの動向 日本の研究が世界リード 原子炉に代わる加速器開発
BNCTは、中性子の発見から4年後の1936年に米国で原理が提唱された。その臨床研究は60年代後半から、日本が世界をリードする形で発展させてきた。
医用原子力技術研究振興財団(東京)によると、2009年1月までに行われたBNCTの治療は国内で525例を数える。治療対象は脳腫瘍、頭頸部がん、皮膚がん、肝臓がん、肺がん、中皮腫、骨・軟部肉腫など。このうち皮膚がん(悪性黒色腫)治療の実施医療機関は全国で川崎医大病院だけ。
BNCTに用いる中性子はこれまで研究用原子炉からしか得られなかった。原子炉は元来医療設備ではなく、保守点検のための長期休止期間、設置場所の制約などがあり、医療として認められるのは不可能に近い。このため原子炉に代わる中性子源として、小型加速器の開発が行われている。加速器は原子炉よりも操作が簡単で、都市の病院内にも設置可能だ。
今年6月から京都大学原子炉実験所で加速器を使ったBNCTの臨床研究が始まる予定。国立がん研究センター中央病院(東京)も昨年1月、「病院設置型の加速器を開発し3年後をめどに臨床研究を開始する」と発表した。平塚教授は「加速器が本格稼働するようになれば、BNCTが一般的治療として、がん治療の一翼を担える日も近い」と言う。
(2012年02月06日 更新)